近日,我院李锦铨课题组在猪链球菌的跨宿主传播的分子机制、地域传播规律以及毒力的进化方面取得了新的进展。该研究首次提出猪链球菌人类适应性种群已经形成,证实了该类菌株的强致病性并建立了针对该类型菌株的检测方法,为有效阻断该病原在食品生产链中的传播和对人类健康造成的威胁提供科学依据。相关科研成果以“The global emergence of a novel Streptococcus suis clade associated with human infections”为题发表在EMBO Molecular Medicine上。
图1 猪链球菌可感染的宿主
猪链球菌是一种致病性的革兰氏阳性菌,其引起的猪链球菌病是一种新发的人畜共患病,可通过猪传人途径传播,导致人类感染并出现脑膜炎、败血症,听力减弱或者丧失,以及罕见的中毒性休克等多种临床症状。越来越多的研究表明猪链球菌的感染宿主的范围在不断的扩大,涵盖野生动物类、家禽类、牲畜类以及宠物类,感染宿主范围的拓展和人群感染率的不断增加表明这种新型病原的环境适应能力和致病性都在不断的进化,提示我们要重视该新发病原,并阻断其在食品生产链中的传播。
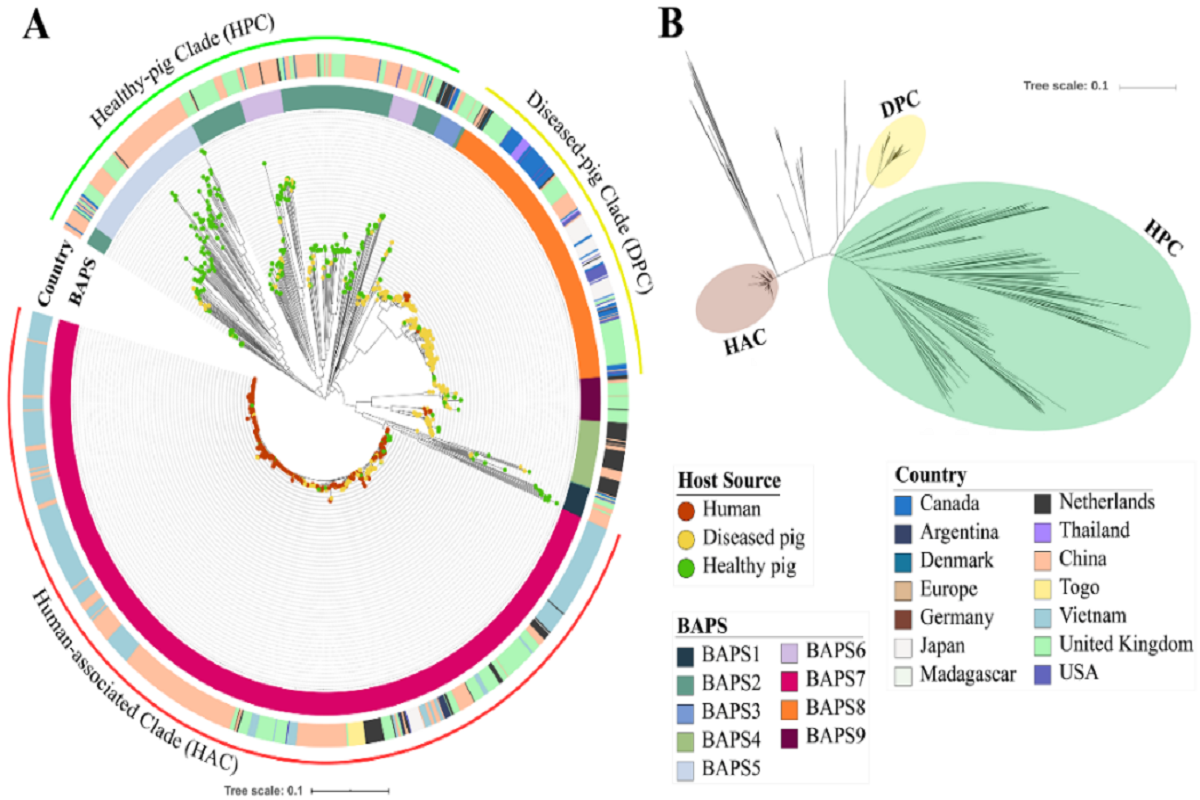
图2 全基因组系统发育树揭示了猪链球菌宿主相关性
研究人员对全世界1634 个菌株的全基因组数据进行了比较基因组学分析,揭示了 3 个与宿主密切相关的种群结构,分别为人类适应性菌株组(HAC,Human-associated Clade)、健康猪组(HPC, Healthy-pig Clade)和病猪组(DPC, Diseased-pig Clade)。研究发现,HAC组的菌株来源于9个不同的国家,说明该类型的菌株已经在全球进行传播和扩散,其中在亚洲形成3个平行进化的流行性支系(Ⅰ、Ⅱ、Ⅲ),其中支系Ⅰ为引起了中国的两次大爆发的中国特有序列型——ST7菌株;支系Ⅱ为ST1型菌株组成,该支系的菌株携带一个与89kb高度类似的78kb的毒力岛,正在中国和越南之间传播;支系Ⅲ为新型的ST7菌株,该支系的菌株携带一个含多类抗性基因的127kb的耐药岛,目前已经在中国境内多个省份发现。支系Ⅱ、Ⅲ为本研究新鉴定的2个支系,需要引起我们高度重视。
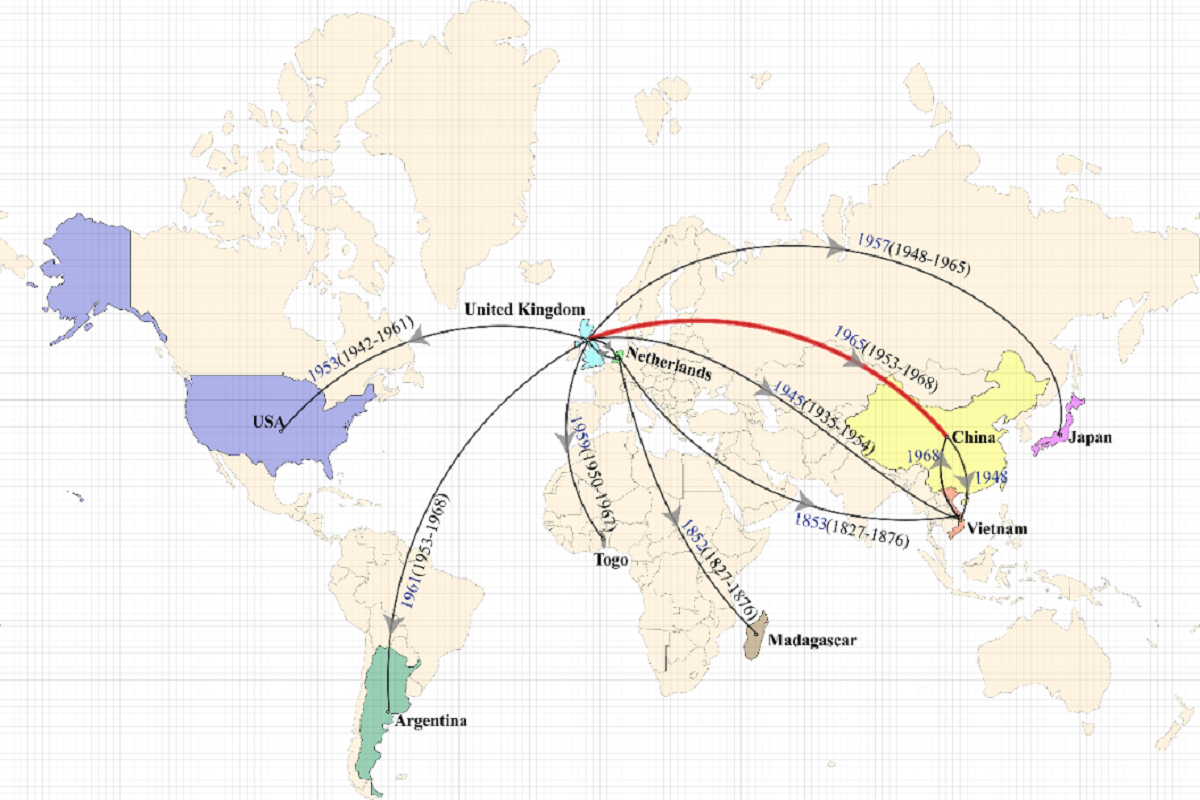
图3 生物地理学推断HAC组菌株全球可能的传播路径
beat365体育亚洲官方网站beat365体育亚洲官方网站研究生董星星和上海巴斯德研究所研究员晁彦杰为本论文共同第一作者。beat365体育亚洲官方网站李锦铨研究员和浙江大学的冯晔副教授为共同通讯作者。本研究获得了国家重点研发计划,国家自然科学基金,湖北省科技创新专项,beat365体育亚洲官方网站校自主创新基金资助。
审核人 刘石林
【英文摘要】
Streptococcus suis, a ubiquitous bacterial colonizer in pigs, has recently extended host range to humans, leading to a global surge of deadly human infections and three large outbreaks since 1998. To better understand the mechanisms for the emergence of crossspecies transmission and virulence in human, we have sequenced 366 S. suis human and pig isolates from 2005 to 2016 and performed a large-scale phylogenomic analysis on 1,634 isolates from 14 countries over 36 years. We show the formation of a novel human-associated clade (HAC) diversified from swine S. suis isolates. Phylogeographic analysis identified Europe as the origin of HAC, coinciding with the exportation of European swine breeds between 1960s and 1970s. HAC is composed of three sub-lineages and contains several healthy-pig isolates that display high virulence experimental infections, suggesting healthy-pig carriers as a potential source for human infection. New HAC-specific genes are identified as promising markers for pathogen detection and surveillance. Our discovery of a human-associated S. suis clade provides insights into the evolution of this emerging human pathogen and extend our understanding of S. suis epidemics worldwide.
原文链接:https://www.embopress.org/doi/full/10.15252/emmm.202013810


